山東埃爾派 | 點擊量:0次 | 2020-12-02
醫(yī)用樹枝狀大分子藥物輔料:合成、性質(zhì)、毒性和生物醫(yī)學(xué)應(yīng)用

歐洲藥品管理局(EMA)和美國現(xiàn)行藥品生產(chǎn)規(guī)范(cGMP)將輔料定義為藥物配方中活性成分以外的組分,即任何可以提供藥理活性的成分。目前,由于沒有關(guān)于樹枝狀分子的藥典專著,這類大分子還不能確認為藥物輔料,但這類納米結(jié)構(gòu)分子引起了極大的關(guān)注。由于其特殊的性質(zhì),如納米級規(guī)整尺寸、支化度高、多價、水溶、有內(nèi)部空穴、生物相容性等,樹枝狀大分子是理想的活性輔料,可增強水溶性差的藥物的溶解性。
樹枝狀分子的性質(zhì)可通過合成控制,這使其成為一些藥物的遞送載體。此外,樹枝狀分子可降低藥物的毒性,提高藥效。這篇綜述討論了樹枝狀分子作為輔料的性質(zhì)及其它們在制藥和生物醫(yī)學(xué)領(lǐng)域的應(yīng)用。
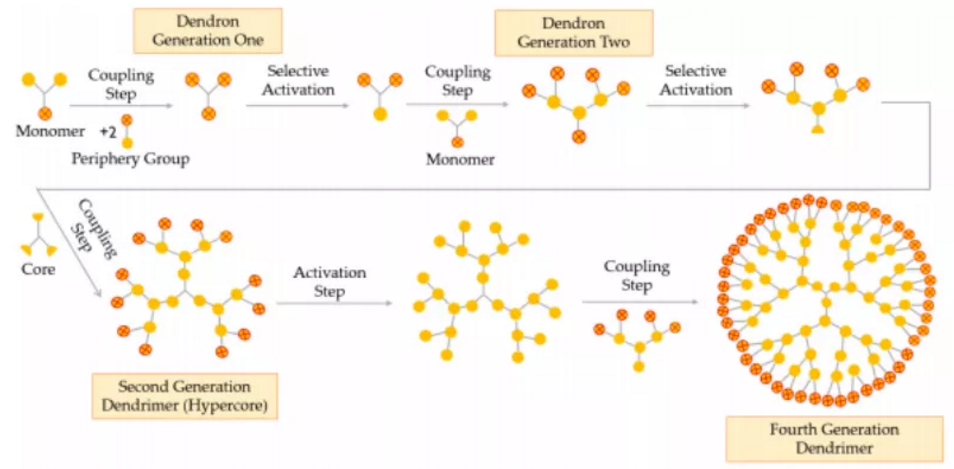
圖1樹枝狀大分子的合成方法
一些藥物活性成分(APIs)由于良好的溶解性和生物膜滲透性而固有生物利 用度。但是,其中許多是屬于生物藥劑學(xué)分類系統(tǒng)(BCS)中的II類,即溶解性低, 滲透性高;或?qū)儆贗V類,即溶解性低,滲透率也低,這會導(dǎo)致其生物利用率低。 由于生物利用度問題,制藥業(yè)開發(fā)的原料藥中有近40%被淘汰。改進API生物利用度缺陷的一種方法是通過在配方中加入適當(dāng)?shù)妮o料以提高藥物的溶解性。
據(jù)報道,樹枝狀大分子可以增加親水與疏水藥物的溶解性。其增溶機理很大 程度上取決于樹枝狀分子的質(zhì)子化與去質(zhì)子化。端氨基PPI、PAMAM具有堿性端 基與內(nèi)部結(jié)構(gòu)。這類樹枝狀分子內(nèi)結(jié)構(gòu)中含有叔氨基,當(dāng)pH<4,其通常為擴展結(jié)構(gòu)。在該pH,由于表面和內(nèi)部結(jié)構(gòu)中帶正電荷氨基間的相互排斥作用,隨著分子代數(shù)增加,分子內(nèi)部空穴增加。此外,在中性pH條件下,由于帶正電荷的表面氨基與內(nèi)結(jié)構(gòu)中不帶電荷的叔胺之間的氫鍵相互作用,分子會出現(xiàn)卷曲構(gòu)象。當(dāng) pH≥10,分子的電荷變成中性,樹枝狀分子就會收縮,形成緊密網(wǎng)絡(luò)的球狀結(jié)構(gòu), 此時分子內(nèi)部基團與端基的排斥作用最低。
樹枝狀分子可以遞送眼部藥物、口服藥物、 靜脈注射藥物、肺部藥物、中樞神經(jīng)系統(tǒng)藥物、透皮給藥、鼻腔給藥、基因投遞、 疫苗等。
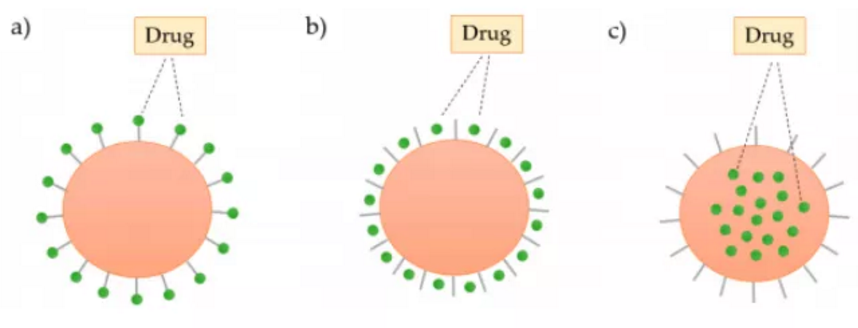
圖2. 樹枝狀大分子與藥物的三種結(jié)合方式,a) 共價連接;b) 靜電相互作用;c)包封
結(jié)論與展望
預(yù)計樹枝狀大分子輔料將在制藥工業(yè)和醫(yī)藥領(lǐng)域發(fā)揮重要作用。由于樹枝狀大分的結(jié)構(gòu)特性(納米級尺寸、高分支度、多價、水溶性、內(nèi)部空腔等)以及結(jié)構(gòu)可控等性質(zhì),其作為輔料可改善配方藥物的性質(zhì)。藥物分子可通過共價連接、靜電作用或包封與樹枝狀大分子結(jié)合。選擇結(jié)合方式取決于藥物的性質(zhì)和病理類型。樹枝狀大分子是理想的藥物載體,可通過設(shè)計用于靶向遞送,所需藥物劑量較小且感染的副作用較小。 另一個已被證明的優(yōu)點是樹枝狀分子納米體系是兼容、安全、有效的納米載體。它可增加具有治療價值但由于水溶性低而被制藥工業(yè)淘汰的藥物范圍。許多研究已經(jīng)表明,樹枝狀大分子在一些治療藥物中是有應(yīng)用前景的藥物輔料。值得注意的是,目前的研究都是在體外模型或動物模型上進行的,盡管這項新技術(shù) 很有前景,但仍需進一步進行與完善人體內(nèi)的試驗研究,以更準確的了解其生物相容性和毒性。
推薦您閱讀粉體行業(yè)資訊、了解工業(yè)產(chǎn)品技術(shù)、熟悉更多超微粉碎產(chǎn)品百科知識,助您選設(shè)備不求人。






















